Abstrak
9,10-Anthraquinone (AQ) ialah bahan cemar dengan potensi risiko karsinogenik dan berlaku dalam teh di seluruh dunia.Had baki maksimum (MRL) AQ dalam teh yang ditetapkan oleh Kesatuan Eropah (EU) ialah 0.02 mg/kg.Sumber kemungkinan AQ dalam pemprosesan teh dan peringkat utama kejadiannya telah disiasat berdasarkan kaedah analisis AQ yang diubah suai dan analisis spektrometri jisim kromatografi-tandem gas (GC-MS/MS).Berbanding dengan elektrik sebagai sumber haba dalam pemprosesan teh hijau, AQ meningkat sebanyak 4.3 hingga 23.9 kali ganda dalam pemprosesan teh dengan arang batu sebagai sumber haba, jauh melebihi 0.02 mg/kg, manakala tahap AQ dalam persekitaran meningkat tiga kali ganda.Trend yang sama diperhatikan dalam pemprosesan teh oolong di bawah haba arang batu.Langkah-langkah dengan sentuhan langsung antara daun teh dan asap, seperti penetapan dan pengeringan, dianggap sebagai langkah utama pengeluaran AQ dalam pemprosesan teh.Tahap AQ meningkat dengan peningkatan masa sentuhan, menunjukkan bahawa tahap pencemar AQ yang tinggi dalam teh mungkin berasal daripada asap yang disebabkan oleh arang batu dan pembakaran.Empat puluh sampel dari bengkel berbeza dengan elektrik atau arang batu sebagai sumber haba dianalisis, berjulat daripada 50.0%−85.0% dan 5.0%−35.0% untuk pengesanan dan melebihi kadar AQ.Di samping itu, kandungan AQ maksimum 0.064 mg/kg diperhatikan dalam produk teh dengan arang batu sebagai sumber haba, menunjukkan bahawa tahap pencemaran AQ yang tinggi dalam produk teh berkemungkinan disumbangkan oleh arang batu.
Kata kunci: 9,10-Antrakuinon, Pemprosesan teh, Arang batu, Sumber pencemaran
PENGENALAN
Teh yang dihasilkan daripada daun pokok renek malar hijau Camellia sinensis (L.) O. Kuntze, merupakan salah satu minuman paling popular di dunia kerana rasa yang menyegarkan dan manfaat kesihatannya.Pada tahun 2020 secara global, pengeluaran teh telah meningkat kepada 5,972 juta tan metrik, yang meningkat dua kali ganda dalam tempoh 20 tahun yang lalu[1].Berdasarkan cara pemprosesan yang berbeza, terdapat enam jenis teh utama, termasuk teh hijau, teh hitam, teh gelap, teh oolong, teh putih dan teh kuning[2,3].Untuk memastikan kualiti dan keselamatan produk, adalah sangat penting untuk memantau tahap bahan pencemar dan menentukan asal usul.
Mengenal pasti sumber bahan cemar, seperti sisa racun perosak, logam berat dan bahan pencemar lain seperti hidrokarbon aromatik polisiklik (PAH), adalah langkah utama untuk mengawal pencemaran.Penyemburan terus bahan kimia sintetik di ladang teh, serta hanyutan udara yang disebabkan oleh operasi berhampiran kebun teh, adalah sumber utama sisa racun perosak dalam teh[4].Logam berat boleh terkumpul dalam teh dan membawa kepada ketoksikan, yang kebanyakannya berasal daripada tanah, baja dan atmosfera[5-7].Bagi pencemaran lain yang muncul secara tidak dijangka dalam teh, agak sukar untuk dikenal pasti kerana prosedur kompleks rantaian pengeluaran teh termasuk perladangan, pemprosesan, pembungkusan, penyimpanan dan pengangkutan.PAH dalam teh berasal daripada pemendapan ekzos kenderaan dan pembakaran bahan api yang digunakan semasa pemprosesan daun teh, seperti kayu api dan arang batu[8-10].
Semasa pembakaran arang batu dan kayu api, bahan pencemar seperti karbon oksida terbentuk[11].Akibatnya, adalah terdedah kepada sisa-sisa bahan pencemar yang disebutkan di atas untuk berlaku dalam produk yang diproses, seperti bijirin, stok asap dan ikan kucing, pada suhu tinggi, yang menimbulkan ancaman kepada kesihatan manusia[12,13].PAH yang disebabkan oleh pembakaran diperoleh daripada pemeruapan PAH yang terkandung dalam bahan api itu sendiri, penguraian suhu tinggi sebatian aromatik dan tindak balas kompaun antara radikal bebas[14].Suhu pembakaran, masa, dan kandungan oksigen adalah faktor penting yang mempengaruhi penukaran PAH.Dengan peningkatan suhu, kandungan PAH mula-mula meningkat dan kemudian menurun, dan nilai puncak berlaku pada 800 °C;Kandungan PAH menurun secara mendadak untuk dikesan dengan peningkatan masa pembakaran apabila ia berada di bawah had yang dipanggil 'masa sempadan', dengan peningkatan kandungan oksigen dalam udara pembakaran, pelepasan PAH berkurangan dengan ketara, tetapi pengoksidaan yang tidak lengkap akan menghasilkan OPAH dan derivatif lain[15]. −17].
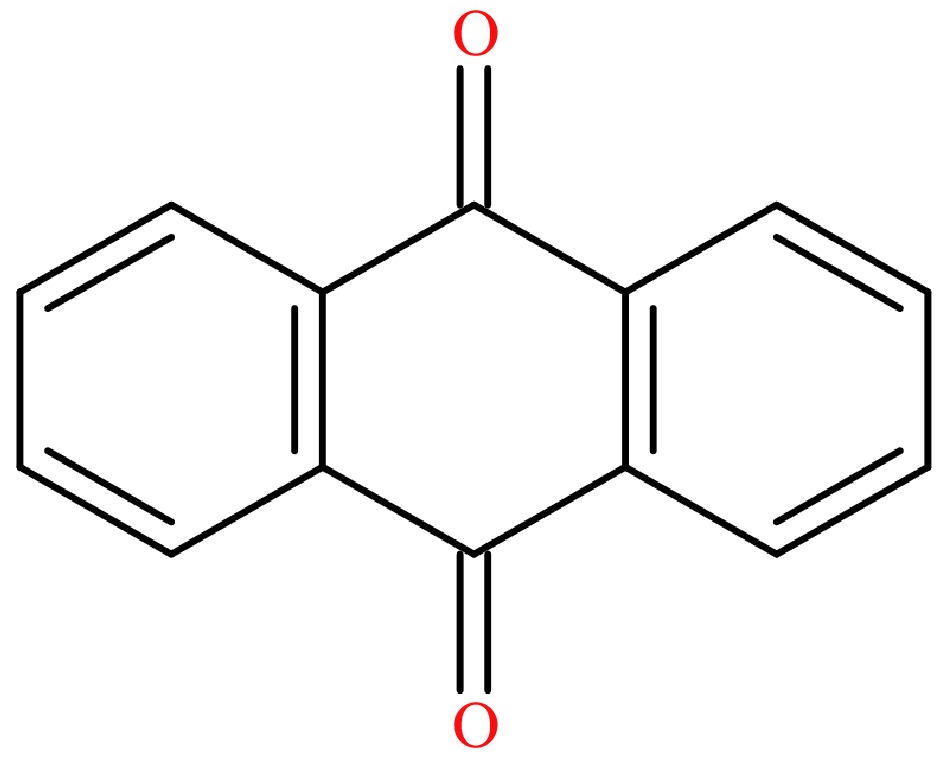
9,10-Antrakuinon (AQ, CAS: 84-65-1, Rajah 1), terbitan yang mengandungi oksigen bagi PAH[18], terdiri daripada tiga kitaran terkondensasi.Ia telah disenaraikan sebagai karsinogen yang mungkin (Kumpulan 2B) oleh Agensi Antarabangsa untuk Penyelidikan Kanser pada 2014[19].AQ boleh meracuni kompleks belahan topoisomerase II dan menghalang hidrolisis adenosin trifosfat (ATP) oleh DNA topoisomerase II, menyebabkan DNA putus rantai ganda, yang bermaksud pendedahan jangka panjang di bawah persekitaran yang mengandungi AQ dan sentuhan langsung dengan tahap AQ yang tinggi boleh menyebabkan kerosakan DNA, mutasi dan meningkatkan risiko kanser[20].Sebagai kesan negatif terhadap kesihatan manusia, had sisa maksimum (MRL) AQ sebanyak 0.02 mg/kg telah ditetapkan dalam teh oleh Kesatuan Eropah.Menurut kajian terdahulu kami, deposit AQ dicadangkan sebagai sumber utama semasa ladang teh[21].Selain itu, berdasarkan akibat eksperimen dalam pemprosesan teh hijau dan hitam Indonesia, adalah jelas bahawa tahap AQ berubah dengan ketara dan asap daripada peralatan pemprosesan dicadangkan sebagai salah satu sebab utama[22].Walau bagaimanapun, asal tepat AQ dalam pemprosesan teh masih sukar difahami, walaupun beberapa hipotesis laluan kimia AQ telah dicadangkan [23,24], menunjukkan bahawa adalah sangat penting untuk menentukan faktor penting yang mempengaruhi tahap AQ dalam pemprosesan teh.
Rajah 1. Formula kimia AQ.
Memandangkan penyelidikan tentang pembentukan AQ semasa pembakaran arang batu dan potensi ancaman bahan api dalam pemprosesan teh, satu eksperimen perbandingan telah dijalankan untuk menerangkan kesan pemprosesan sumber haba ke atas AQ dalam teh dan udara, analisis kuantitatif terhadap perubahan kandungan AQ. pada langkah pemprosesan yang berbeza, yang membantu untuk mengesahkan asal tepat, corak kejadian dan tahap pencemaran AQ dalam pemprosesan teh.
KEPUTUSAN
Pengesahan kaedah
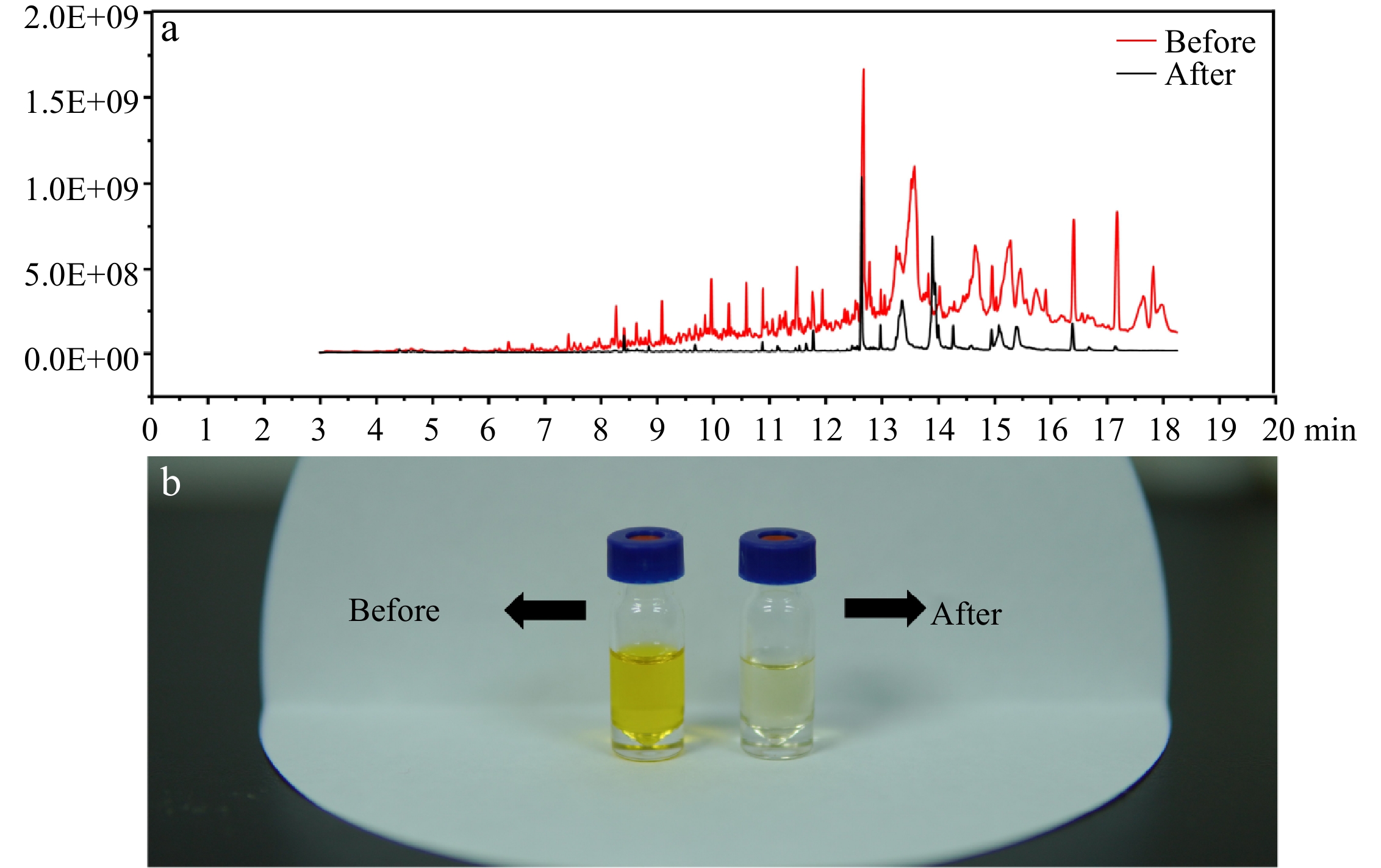
Berbanding dengan kajian terdahulu kami [21], prosedur pengekstrakan cecair-cecair telah digabungkan sebelum suntikan kepada GC-MS/MS untuk meningkatkan kepekaan dan mengekalkan pernyataan instrumental.Dalam Rajah 2b, kaedah yang ditambah baik menunjukkan peningkatan yang ketara dalam penulenan sampel, pelarut menjadi lebih cerah dalam warna.Dalam Rajah 2a, spektrum imbasan penuh (50−350 m/z) menggambarkan bahawa selepas penulenan, garis asas spektrum MS berkurangan dengan jelas dan puncak kromatografi yang lebih sedikit tersedia, menunjukkan bahawa sejumlah besar sebatian mengganggu telah dikeluarkan selepas pengekstrakan cecair-cecair.
Rajah 2. (a) Spektrum imbasan penuh sampel sebelum dan selepas penulenan.(b) Kesan penulenan kaedah yang dipertingkatkan.
Pengesahan kaedah, termasuk kelinearan, pemulihan, had kuantiti (LOQ) dan kesan matriks (ME), ditunjukkan dalam Jadual 1. Adalah memuaskan untuk mendapatkan kelinearan dengan pekali penentuan (r2) lebih tinggi daripada 0.998, yang berjulat dari 0.005 hingga 0.2 mg/kg dalam matriks teh dan pelarut asetonitril, dan dalam sampel udara dengan julat 0.5 hingga 8 μg/m3.
Pemulihan AQ dinilai pada tiga kepekatan berduri antara kepekatan yang diukur dan sebenar dalam teh kering (0.005, 0.02, 0.05 mg/kg), pucuk teh segar (0.005, 0.01, 0.02 mg/kg) dan sampel udara (0.5, 1.5, 3). μg/m3).Pemulihan AQ dalam teh adalah antara 77.78% hingga 113.02% dalam teh kering dan dari 96.52% hingga 125.69% dalam pucuk teh, dengan RSD% lebih rendah daripada 15%.Pemulihan AQ dalam sampel udara adalah antara 78.47% hingga 117.06% dengan RSD% di bawah 20%.Kepekatan pancang yang paling rendah dikenal pasti sebagai LOQ, iaitu 0.005 mg/kg, 0.005 mg/kg dan 0.5 μg/m³ dalam pucuk teh, teh kering dan sampel udara, masing-masing.Seperti yang disenaraikan dalam Jadual 1, matriks teh kering dan pucuk teh sedikit meningkatkan tindak balas AQ, membawa kepada ME sebanyak 109.0% dan 110.9%.Bagi matriks sampel udara, ME ialah 196.1%.
Tahap AQ semasa pemprosesan teh hijau
Dengan tujuan untuk mengetahui kesan sumber haba yang berbeza pada teh dan persekitaran pemprosesan, sekumpulan daun segar dibahagikan kepada dua kumpulan tertentu dan diproses secara berasingan di dua bengkel pemprosesan di perusahaan yang sama.Satu kumpulan dibekalkan dengan elektrik, dan satu lagi dengan arang batu.
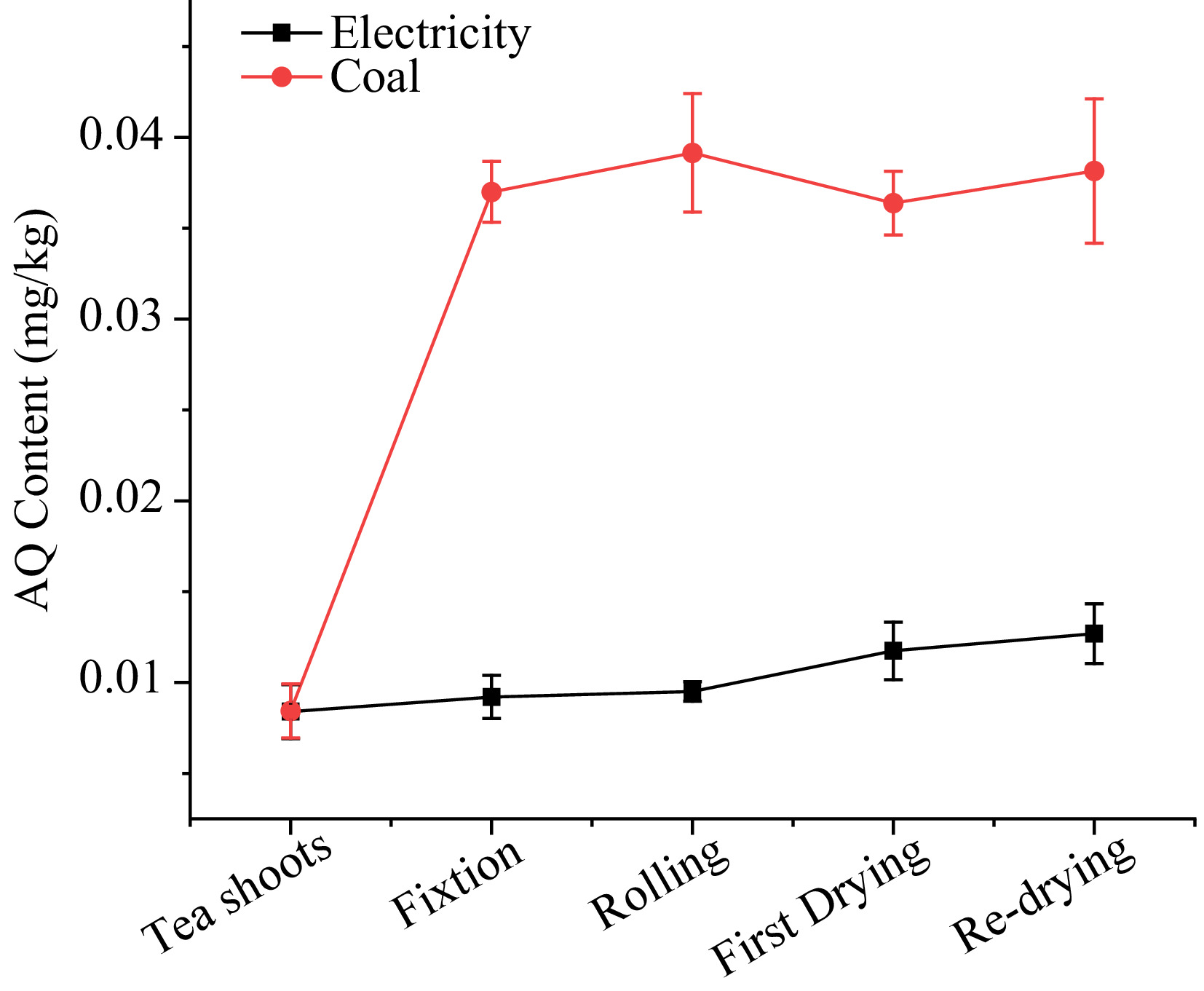
Seperti yang ditunjukkan dalam Rajah 3, paras AQ dengan elektrik sebagai sumber haba adalah antara 0.008 hingga 0.013 mg/kg.Semasa proses penetapan, pengeringan daun teh yang disebabkan oleh pemprosesan dalam periuk dengan suhu tinggi menghasilkan peningkatan 9.5% dalam AQ.Kemudian, tahap AQ kekal semasa proses penggulungan walaupun kehilangan jus, menunjukkan bahawa proses fizikal mungkin tidak menjejaskan tahap AQ dalam pemprosesan teh.Selepas langkah pengeringan pertama, tahap AQ meningkat sedikit daripada 0.010 kepada 0.012 mg/kg, kemudian terus meningkat kepada 0.013 mg/kg sehingga akhir pengeringan semula.PF, yang menunjukkan variasi secara signifikan dalam setiap langkah, masing-masing ialah 1.10, 1.03, 1.24, 1.08 dalam penetapan, penggelek, pengeringan pertama dan pengeringan semula.Keputusan PF mencadangkan bahawa pemprosesan di bawah tenaga elektrik mempunyai sedikit kesan pada tahap AQ dalam teh.
Rajah 3. Tahap AQ semasa pemprosesan teh hijau dengan elektrik dan arang batu sebagai sumber haba.
Dalam kes arang batu sebagai sumber haba, kandungan AQ meningkat secara mendadak semasa pemprosesan teh, melonjak daripada 0.008 kepada 0.038 mg/kg.338.9% AQ telah meningkat dalam prosedur penetapan, mencapai 0.037 mg/kg, yang jauh melebihi MRL 0.02 mg/kg yang ditetapkan oleh Kesatuan Eropah.Semasa peringkat rolling, tahap AQ masih meningkat sebanyak 5.8% walaupun jauh dari mesin penetapan.Dalam pengeringan pertama dan pengeringan semula, kandungan AQ meningkat sedikit atau berkurangan sedikit.PF yang menggunakan arang batu sebagai sumber haba dalam penetapan, pengeringan gulung pertama dan pengeringan semula masing-masing ialah 4.39, 1.05, 0.93, dan 1.05.
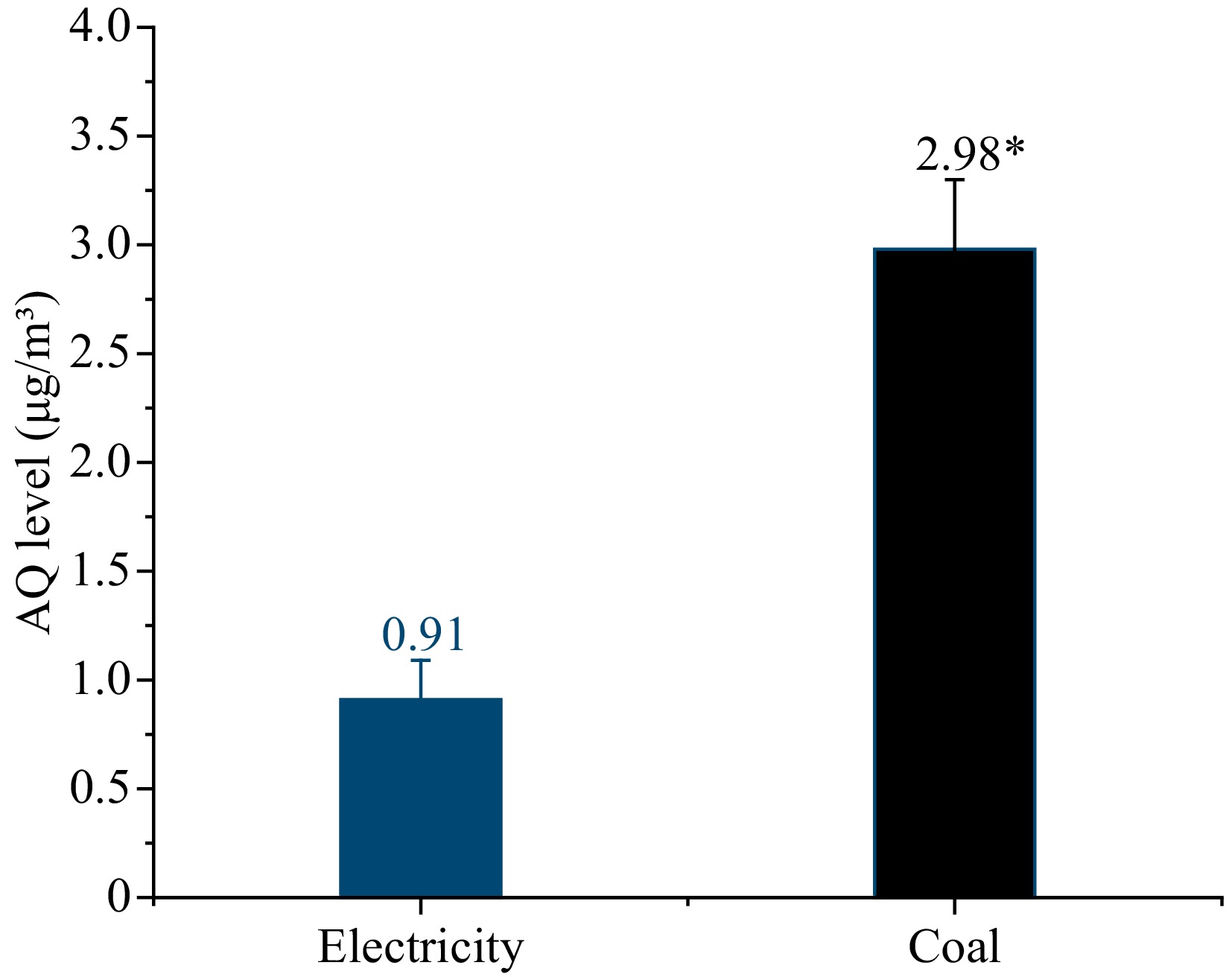
Untuk menentukan lebih lanjut hubungan antara pembakaran arang batu dan pencemaran AQ, bahan zarah terampai (PMs) dalam udara di bengkel di bawah kedua-dua sumber haba telah dikumpulkan untuk penilaian udara, seperti ditunjukkan dalam Rajah 4. Tahap AQ PM dengan arang batu sebagai sumber haba ialah 2.98 μg/m3, iaitu lebih tiga kali ganda lebih tinggi daripada itu dengan elektrik 0.91 μg/m3.
Rajah 4. Tahap AQ dalam persekitaran dengan elektrik dan arang batu sebagai sumber haba.* Menunjukkan perbezaan ketara dalam tahap AQ dalam sampel (p < 0.05).
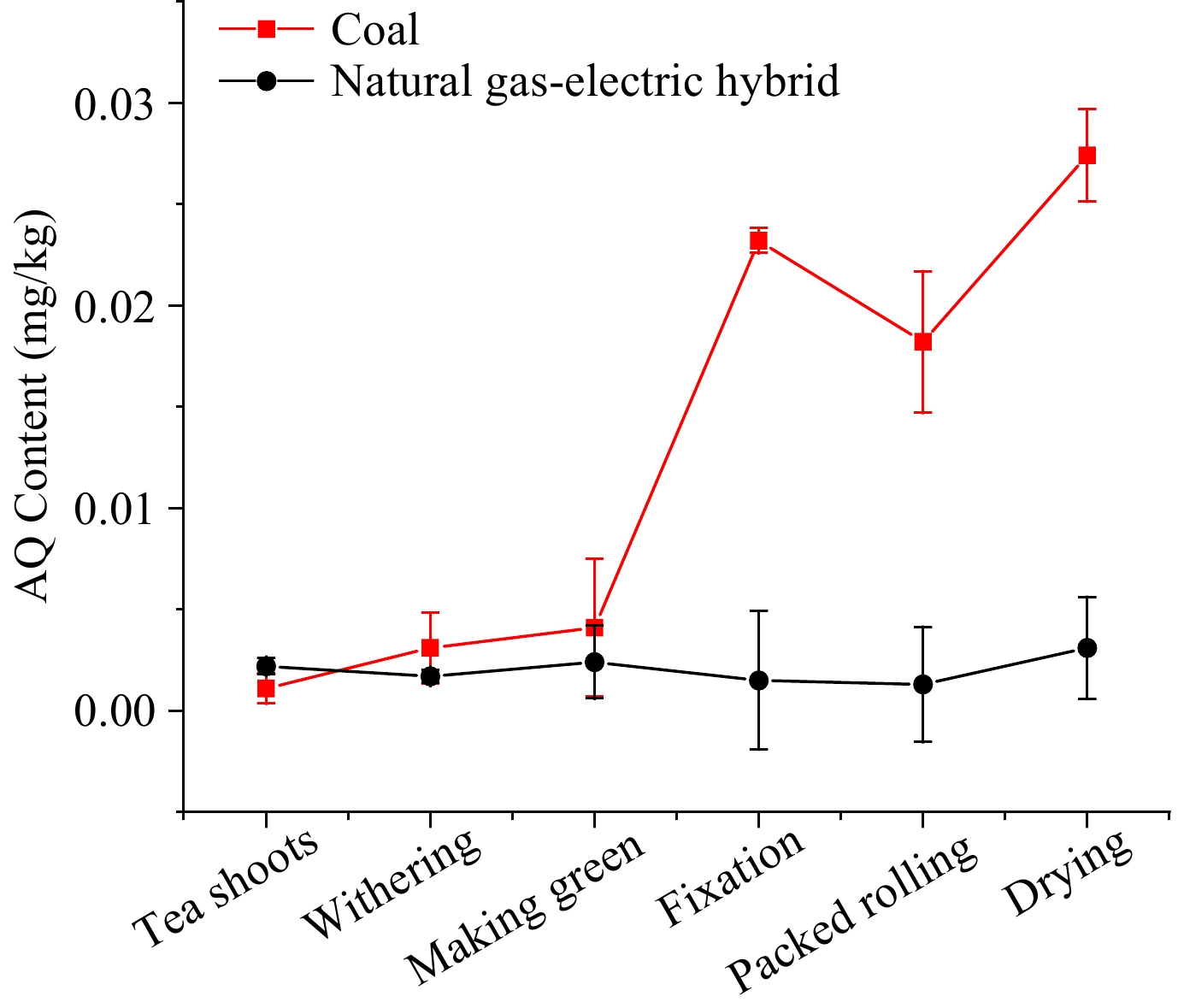
Tahap AQ semasa pemprosesan teh oolong Teh oolong, terutamanya dihasilkan di Fujian dan Taiwan, adalah sejenis teh yang ditapai separa.Untuk menentukan lebih lanjut langkah-langkah utama meningkatkan tahap AQ dan kesan bahan api yang berbeza, kumpulan daun segar yang sama telah dibuat menjadi teh oolong dengan arang batu dan hibrid gas asli-elektrik sebagai sumber haba, secara serentak.Tahap AQ dalam pemprosesan teh oolong menggunakan sumber haba yang berbeza ditunjukkan dalam Rajah. 5. Untuk pemprosesan teh oolong dengan hibrid gas-elektrik asli, arah aliran tahap AQ adalah bertakung di bawah 0.005 mg/kg, yang serupa dengan teh hijau. dengan elektrik.
Rajah 5. Tahap AQ semasa pemprosesan teh oolong dengan campuran gas asli-elektrik dan arang batu sebagai sumber haba.
Dengan arang batu sebagai sumber haba, paras AQ dalam dua langkah pertama, layu dan menjadi hijau, pada asasnya adalah sama seperti campuran gas asli-elektrik.Walau bagaimanapun, prosedur seterusnya sehingga penetapan menunjukkan jurang melebar secara beransur-ansur, di mana tahap AQ melonjak daripada 0.004 kepada 0.023 mg/kg.Tahap dalam langkah guling yang dibungkus menurun kepada 0.018 mg/kg, yang mungkin disebabkan oleh kehilangan jus teh yang membawa pergi beberapa bahan cemar AQ.Selepas peringkat rolling, tahap dalam peringkat pengeringan meningkat kepada 0.027 mg/kg.Dalam layu, membuat hijau, penetapan, penggelek berbungkus dan pengeringan, PF masing-masing adalah 2.81, 1.32, 5.66, 0.78, dan 1.50.
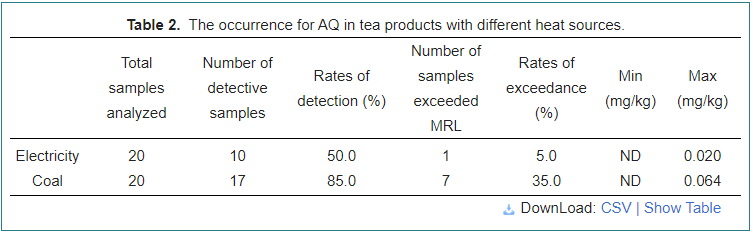
Kejadian AQ dalam produk teh dengan sumber haba yang berbeza
Untuk menentukan kesan ke atas kandungan AQ teh dengan sumber haba yang berbeza, 40 sampel teh dari bengkel teh menggunakan elektrik atau arang batu sebagai sumber haba telah dianalisis, seperti ditunjukkan dalam Jadual 2. Berbanding dengan menggunakan elektrik sebagai sumber haba, arang batu mempunyai paling banyak kadar detektif (85.0%) dengan tahap AQ maksimum 0.064 mg/kg, menunjukkan bahawa ia adalah mudah untuk menyebabkan pencemar AQ oleh asap yang dihasilkan oleh pembakaran arang batu, dan kadar 35.0% diperhatikan dalam sampel arang batu.Paling ketara, elektrik mempunyai kadar detektif dan eksesan terendah masing-masing sebanyak 56.4% dan 7.7%, dengan kandungan maksimum 0.020 mg/kg.
PERBINCANGAN
Berdasarkan PF semasa pemprosesan dengan dua jenis sumber haba, adalah jelas bahawa penetapan adalah langkah utama yang membawa kepada peningkatan tahap AQ dalam pengeluaran teh dengan arang batu dan pemprosesan di bawah tenaga elektrik mempunyai sedikit kesan ke atas kandungan AQ. dalam teh.Semasa pemprosesan teh hijau, pembakaran arang batu menghasilkan banyak asap dalam proses penetapan berbanding dengan proses pemanasan elektrik, menunjukkan bahawa mungkin asap adalah sumber utama pencemar AQ daripada sentuhan dengan pucuk teh serta-merta dalam pemprosesan teh, sama seperti proses pendedahan dalam sampel barbeku salai[25].Peningkatan sedikit dalam kandungan AQ semasa peringkat rolling mencadangkan bahawa asap yang disebabkan oleh pembakaran arang batu bukan sahaja menjejaskan tahap AQ semasa langkah penetapan, tetapi juga dalam persekitaran pemprosesan akibat pemendapan atmosfera.Arang batu juga digunakan sebagai sumber haba dalam pengeringan pertama dan pengeringan semula, tetapi dalam dua langkah ini kandungan AQ meningkat sedikit atau berkurangan sedikit.Ini mungkin dijelaskan oleh fakta bahawa pengering angin panas tertutup menyimpan teh daripada asap yang disebabkan oleh pembakaran arang batu[26].Untuk menentukan sumber pencemar, tahap AQ di atmosfera telah dianalisis, menghasilkan jurang yang ketara antara kedua-dua bengkel.Sebab utama untuk ini ialah arang batu yang digunakan dalam peringkat penetapan, pengeringan pertama dan pengeringan semula akan menjana AQ semasa pembakaran tidak lengkap.AQ ini kemudiannya diserap dalam zarah kecil pepejal selepas pembakaran arang batu dan tersebar di udara, meningkatkan tahap pencemaran AQ dalam persekitaran bengkel[15].Dari masa ke masa, disebabkan oleh luas permukaan khusus yang besar dan kapasiti penjerapan teh, zarah-zarah ini kemudiannya mengendap di permukaan daun teh, mengakibatkan peningkatan AQ dalam pengeluaran.Oleh itu, pembakaran arang batu dianggap sebagai laluan utama yang membawa kepada pencemaran AQ yang berlebihan dalam pemprosesan teh, dengan asap menjadi punca pencemaran.
Bagi pemprosesan teh oolong, AQ telah meningkat di bawah pemprosesan dengan kedua-dua sumber haba, tetapi perbezaan antara kedua-dua sumber haba adalah ketara.Keputusan juga mencadangkan bahawa arang batu sebagai sumber haba memainkan peranan utama dalam meningkatkan tahap AQ, dan penetapan itu dianggap sebagai langkah utama untuk meningkatkan pencemaran AQ dalam pemprosesan teh oolong berdasarkan PF.Semasa pemprosesan teh oolong dengan hibrid gas asli-elektrik sebagai sumber haba, arah aliran tahap AQ tidak berubah di bawah 0.005 mg/kg, yang serupa dengan teh hijau dengan elektrik, menunjukkan bahawa tenaga bersih, seperti elektrik dan semula jadi. gas, boleh mengurangkan risiko menghasilkan bahan cemar AQ daripada pemprosesan.
Bagi ujian pensampelan, keputusan menunjukkan bahawa keadaan pencemaran AQ adalah lebih teruk apabila menggunakan arang batu sebagai sumber haba berbanding elektrik, yang mungkin disebabkan oleh asap daripada pembakaran arang batu yang bersentuhan dengan daun teh dan berlarutan di sekitar tempat kerja.Walau bagaimanapun, walaupun jelas bahawa elektrik adalah sumber haba paling bersih semasa pemprosesan teh, masih terdapat pencemar AQ dalam produk teh yang menggunakan elektrik sebagai sumber haba.Keadaan ini kelihatan sedikit serupa dengan kerja yang diterbitkan sebelum ini di mana tindak balas 2- alkenal dengan hidrokuinon dan benzokuinon dicadangkan sebagai laluan kimia yang berpotensi[23], sebab untuk ini akan disiasat dalam penyelidikan masa depan.
KESIMPULAN
Dalam kerja ini, kemungkinan sumber pencemaran AQ dalam teh hijau dan oolong telah disahkan oleh eksperimen perbandingan berdasarkan kaedah analisis GC-MS/MS yang dipertingkatkan.Penemuan kami secara langsung menyokong bahawa sumber pencemar utama tahap AQ yang tinggi adalah asap yang disebabkan oleh pembakaran, yang bukan sahaja menjejaskan peringkat pemprosesan tetapi juga menjejaskan persekitaran bengkel.Tidak seperti peringkat bergolek dan layu, di mana perubahan dalam tahap AQ tidak ketara, peringkat dengan penglibatan langsung arang batu dan kayu api, seperti penetapan, adalah proses utama di mana pencemaran AQ meningkat disebabkan oleh jumlah sentuhan antara teh. dan asap semasa peringkat ini.Oleh itu, bahan api bersih seperti gas asli dan elektrik disyorkan sebagai sumber haba dalam pemprosesan teh.Selain itu, keputusan eksperimen juga menunjukkan bahawa jika tiada asap yang dihasilkan oleh pembakaran, masih terdapat faktor lain yang menyumbang untuk mengesan AQ semasa pemprosesan teh, manakala sejumlah kecil AQ juga diperhatikan dalam bengkel dengan bahan api bersih, yang perlu disiasat lebih lanjut. dalam penyelidikan masa hadapan.
BAHAN DAN KAEDAH
Reagen, bahan kimia dan bahan
Standard Anthraquinone (99.0%) telah dibeli daripada Syarikat Dr. Ehrenstorfer GmbH (Augsburg, Jerman).Piawaian dalaman D8-Anthraquinone (98.6%) dibeli daripada Isotop C/D/N (Quebec, Kanada).Natrium sulfat kontang (Na2SO4) dan magnesium sulfat (MgSO4) (Shanghai, China).Florisil dibekalkan oleh Syarikat Kimia Organik Wenzhou (Wenzhou, China).Kertas gentian kaca cermin (90 mm) telah dibeli daripada syarikat Ahlstrom-munksjö (Helsinki, Finland).
Penyediaan sampel
Sampel teh hijau diproses dengan penetapan, penggulungan, pengeringan pertama dan pengeringan semula (menggunakan peralatan tertutup), manakala sampel teh oolong diproses dengan layu, menjadikan hijau (goyang dan berdiri daun segar berselang-seli), penetapan, penggelek yang dibungkus, dan pengeringan.Sampel dari setiap langkah dikumpul tiga kali pada 100g selepas pencampuran menyeluruh.Semua sampel disimpan pada suhu -20 ° C untuk analisis lanjut.
Sampel udara dikumpul dengan kertas gentian kaca (90 mm) menggunakan pensampel volum sederhana (PTS-100, Syarikat Alat Elektronik Qingdao Laoshan, Qingdao, China)[27], berjalan pada 100 L/min selama 4 jam.
Sampel yang diperkaya telah dicucuk dengan AQ pada 0.005 mg/kg, 0.010 mg/kg, 0.020 mg/kg untuk pucuk teh segar, pada 0.005 mg/kg, 0.020 mg/kg, 0.050 mg/kg untuk teh kering dan pada 0.012 mg/kg (0.5 µg/m3 untuk sampel udara), 0.036 mg/kg (1.5 µg/m3 untuk smaple udara), 0.072 mg/kg (3.0 µg/m3 untuk sampel udara) untuk kertas penapis kaca, masing-masing.Selepas digoncang dengan teliti, semua sampel dibiarkan selama 12 jam, diikuti dengan langkah pengekstrakan dan pembersihan.
Kandungan lembapan diperoleh dengan mengambil 20 g sampel selepas mencampurkan setiap langkah, dipanaskan pada 105 °C selama 1 jam, kemudian ditimbang dan diulang tiga kali dan mengambil nilai purata dan membahagikannya dengan berat sebelum dipanaskan.
Pengekstrakan sampel dan pembersihan
Sampel teh: Pengekstrakan dan penulenan AQ daripada sampel teh dilakukan berdasarkan kaedah yang diterbitkan daripada Wang et al.dengan beberapa penyesuaian[21].Secara ringkas, 1.5 g sampel teh mula-mula dicampur dengan 30 μL D8-AQ (2 mg/kg) dan dibiarkan selama 30 minit, kemudian dicampur dengan baik dengan 1.5 mL air ternyahion dan dibiarkan selama 30 minit.15 mL 20% aseton dalam n-heksana telah ditambah kepada sampel teh dan disonikasi selama 15 minit.Kemudian sampel dipusingkan dengan 1.0 g MgSO4 selama 30 saat, dan disentrifugasi selama 5 minit, pada 11,000 rpm.Selepas dialihkan ke 100 mL kelalang berbentuk pir, 10 mL fasa organik atas disejat hingga hampir kering di bawah vakum pada 37 °C.5 mL 2.5% aseton dalam n-heksana melarutkan semula ekstrak dalam kelalang berbentuk pir untuk penulenan.Lajur kaca (10 cm × 0.8 cm) terdiri dari bawah ke atas bulu kaca dan 2g florisil, yang berada di antara dua lapisan 2 cm Na2SO4.Kemudian 5 mL 2.5% aseton dalam n-heksana telah membasuh lajur tersebut.Selepas memuatkan larutan terlarut semula, AQ dielusi tiga kali dengan 5 mL, 10 mL, 10 mL 2.5% aseton dalam n-heksana.Eluat gabungan telah dipindahkan ke dalam kelalang berbentuk pir dan disejat sehingga hampir kering di bawah vakum pada 37 °C.Sisa kering kemudiannya disusun semula dengan 1 mL 2.5% aseton dalam heksana diikuti dengan penapisan melalui penapis saiz liang 0.22 µm.Kemudian larutan terlarut itu dicampur dengan asetonitril pada nisbah isipadu 1:1.Mengikuti langkah goncangan, subnatan digunakan untuk analisis GC-MS/MS.
Sampel udara: Separuh daripada kertas gentian, dititiskan dengan 18 μL d8-AQ (2 mg/kg), direndam dalam 15 mL 20% aseton dalam n-heksana, kemudian disonikasikan selama 15 minit.Fasa organik diasingkan dengan sentrifugasi pada 11,000 rpm selama 5 minit dan seluruh lapisan atas dikeluarkan dalam kelalang berbentuk pir.Semua fasa organik telah disejat hingga hampir kering di bawah vakum pada 37 °C.5 mL 2.5% aseton dalam heksana melarutkan semula ekstrak untuk penulenan dengan cara yang sama seperti dalam sampel teh.
Analisis GC-MS/MS
Kromatografi gas Varian 450 yang dilengkapi dengan pengesan jisim tandem Varian 300 (Varian, Walnut Creek, CA, USA) telah digunakan untuk melakukan analisis AQ dengan perisian MS WorkStation versi 6.9.3.Faktor Varian Empat lajur kapilari VF-5ms (30 m × 0.25 mm × 0.25 μm) telah digunakan untuk pengasingan kromatografi.Gas pembawa, helium (> 99.999%), ditetapkan pada kadar aliran malar 1.0 mL/min dengan gas perlanggaran Argon (> 99.999%).Suhu ketuhar bermula dari 80 °C dan ditahan selama 1 minit;meningkat pada 15 °C/min kepada 240 °C, kemudian mencapai 260 °C pada 20 °C/min dan ditahan selama 5min.Suhu sumber ion ialah 210 °C, serta suhu garisan pemindahan 280 °C.Isipadu suntikan ialah 1.0 μL.Keadaan MRM ditunjukkan dalam Jadual 3.
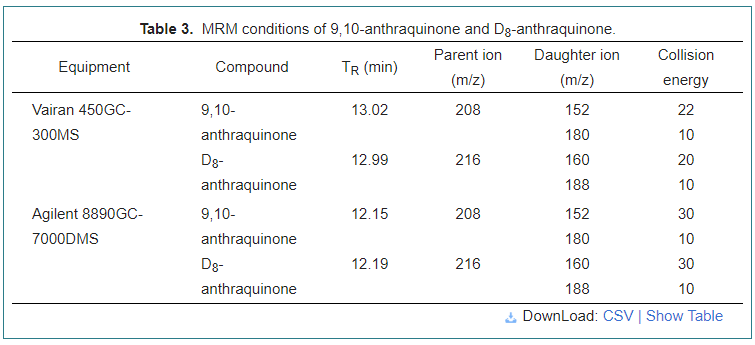
Kromatografi gas Agilent 8890 yang dilengkapi dengan spektrometer jisim triple quadrupole Agilent 7000D (Agilent, Stevens Creek, CA, USA) digunakan untuk menganalisis kesan penulenan dengan perisian MassHunter versi 10.1.Agilent J&W HP-5ms GC Column (30 m × 0.25 mm × 0.25 μm) telah digunakan untuk pengasingan kromatografi.Gas pembawa, Helium (> 99.999%), ditetapkan pada kadar aliran malar 2.25 mL/min dengan gas perlanggaran Nitrogen (> 99.999%).Suhu sumber ion EI telah dilaraskan pada 280 °C, sama seperti suhu garisan pemindahan.Suhu ketuhar bermula dari 80 °C dan ditahan selama 5 minit;dinaikkan sebanyak 15 °C/min kepada 240 °C, kemudian mencapai 280 °C pada 25 °C/min dan dikekalkan selama 5 minit.Keadaan MRM ditunjukkan dalam Jadual 3.
Analisis statistik
Kandungan AQ dalam daun segar telah diperbetulkan kepada kandungan bahan kering dengan membahagikan dengan kandungan lembapan untuk membandingkan dan menganalisis tahap AQ semasa pemprosesan.
Perubahan AQ dalam sampel teh telah dinilai dengan perisian Microsoft Excel dan IBM SPSS Statistics 20.
Faktor pemprosesan digunakan untuk menerangkan perubahan dalam AQ semasa pemprosesan teh.PF = Rl/Rf , di mana Rf ialah aras AQ sebelum langkah pemprosesan dan Rl ialah aras AQ selepas langkah pemprosesan.PF menunjukkan penurunan (PF < 1) atau peningkatan (PF > 1) dalam baki AQ semasa langkah pemprosesan tertentu.
ME menunjukkan penurunan (ME < 1) atau peningkatan (ME > 1) sebagai tindak balas kepada instrumen analisis, yang berdasarkan nisbah cerun penentukuran dalam matriks dan pelarut seperti berikut:
ME = (slopematriks/slopesolvent − 1) × 100%
Di mana slopematrix ialah cerun lengkung penentukuran dalam pelarut dipadankan matriks, slopematrix ialah cerun lengkung penentukuran dalam pelarut.
PENGHARGAAN
Kerja ini disokong oleh Projek Utama Sains dan Teknologi di Wilayah Zhejiang (2015C12001) dan Yayasan Sains Kebangsaan China (42007354).
Konflik kepentingan
Penulis mengisytiharkan bahawa mereka tidak mempunyai konflik kepentingan.
Hak dan kebenaran
Hak Cipta: © 2022 oleh pengarang.Akhbar Akademik Maksimum Pemegang Lesen Eksklusif, Fayetteville, GA.Artikel ini ialah artikel akses terbuka yang diedarkan di bawah Lesen Atribusi Creative Commons (CC BY 4.0), lawati https://creativecommons.org/licenses/by/4.0/.
RUJUKAN
[1] ITC.2021. Buletin Tahunan Perangkaan 2021. https://inttea.com/publication/
[2] Hicks A. 2001. Kajian semula pengeluaran teh global dan kesan kepada industri keadaan ekonomi Asia.Jurnal Teknologi AU 5
Google Scholar
[3] Katsuno T, Kasuga H, Kusano Y, Yaguchi Y, Tomomura M, et al.2014. Pencirian sebatian bau dan pembentukan biokimianya dalam teh hijau dengan proses penyimpanan suhu rendah.Kimia Makanan 148:388−95 doi: 10.1016/j.foodchem.2013.10.069
CrossRef Google Scholar
[4] Chen Z, Ruan J, Cai D, Zhang L. 2007. Rantai Pencemaran Tri-dimensi dalam Ekosistem Teh dan Kawalannya.Scientia Agricultura Sinica 40:948−58
Google Scholar
[5] He H, Shi L, Yang G, You M, Vasseur L. 2020. Penilaian risiko ekologi logam berat tanah dan sisa racun perosak di ladang teh.Pertanian 10:47 doi: 10.3390/pertanian10020047
CrossRef Google Scholar
[6] Jin C, He Y, Zhang K, Zhou G, Shi J, et al.2005. Pencemaran plumbum dalam daun teh dan faktor bukan edafik yang mempengaruhinya.Chemosfera 61:726−32 doi: 10.1016/j.chemosphere.2005.03.053
CrossRef Google Scholar
[7] Owuor PO, Obaga SO, Othieno CO. 1990. Kesan ketinggian pada komposisi kimia teh hitam.Jurnal Sains Makanan dan Pertanian 50:9−17 doi: 10.1002/jsfa.2740500103
CrossRef Google Scholar
[8] Garcia Londoño VA, Reynoso M, Resnik S. 2014. Hidrokarbon aromatik polisiklik (PAH) dalam pasangan yerba (Ilex paraguariensis) dari pasaran Argentina.Bahan Tambahan & Bahan Pencemar Makanan: Bahagian B 7:247−53 doi: 10.1080/19393210.2014.919963
CrossRef Google Scholar
[9] Ishizaki A, Saito K, Hanioka N, Narimatsu S, Kataoka H. 2010. Penentuan hidrokarbon aromatik polisiklik dalam sampel makanan melalui pengekstrakan mikro fasa pepejal dalam tiub dalam talian automatik ditambah dengan pengesanan kromatografi cecair berprestasi tinggi-pendarfluor .Jurnal Kromatografi A 1217:5555−63 doi: 10.1016/j.chroma.2010.06.068
CrossRef Google Scholar
[10] Phan Thi LA, Ngoc NT, Quynh NT, Thanh NV, Kim TT, et al.2020. Hidrokarbon aromatik polisiklik (PAH) dalam daun teh kering dan infusi teh di Vietnam: tahap pencemaran dan penilaian risiko diet.Geokimia dan Kesihatan Persekitaran 42:2853−63 doi: 10.1007/s10653-020-00524-3
CrossRef Google Scholar
[11] Zelinkova Z, Wenzl T. 2015. Kejadian 16 EPA PAH dalam makanan – Kajian semula.Sebatian aromatik polisiklik 35:248−84 doi: 10.1080/10406638.2014.918550
CrossRef Google Scholar
[12] Omodara NB, Olabemiwo OM, Adedosu TA .2019. Perbandingan PAH yang terbentuk dalam kayu api dan stok salai arang dan ikan kucing.Jurnal Sains dan Teknologi Makanan Amerika 7:86−93 doi: 10.12691/ajfst-7-3-3
CrossRef Google Scholar
[13] Zou LY, Zhang W, Atkiston S. 2003. Pencirian pelepasan hidrokarbon aromatik polisiklik daripada pembakaran spesies kayu api yang berbeza di Australia.Pencemaran Alam Sekitar 124:283−89 doi: 10.1016/S0269-7491(02)00460-8
CrossRef Google Scholar
[14] Charles GD, Bartels MJ, Zacharewski TR, Gollapudi BB, Freshour NL, et al.2000. Aktiviti benzo [a] pyrene dan metabolit terhidroksilasinya dalam ujian gen wartawan reseptor-α estrogen.Sains Toksikologi 55:320−26 doi: 10.1093/toxsci/55.2.320
CrossRef Google Scholar
[15] Han Y, Chen Y, Ahmad S, Feng Y, Zhang F, et al.2018. Pengukuran PM dan komposisi kimia yang diselesaikan dengan masa dan saiz yang tinggi daripada pembakaran arang batu: implikasi untuk proses pembentukan EC.Sains & Teknologi Alam Sekitar 52:6676−85 doi: 10.1021/acs.est.7b05786
CrossRef Google Scholar
[16] Khiadani (Hajian) M, Amin MM, Beik FM, Ebrahimi A, Farhadkhani M, et al.2013. Penentuan kepekatan hidrokarbon aromatik polisiklik dalam lapan jenama teh hitam yang digunakan lebih banyak di Iran.Jurnal Antarabangsa Kejuruteraan Kesihatan Persekitaran 2:40 doi: 10.4103/2277-9183.122427
CrossRef Google Scholar
[17] Fitzpatrick EM, Ross AB, Bates J, Andrews G, Jones JM, et al.2007. Pembebasan spesies beroksigen daripada pembakaran kayu pain dan kaitannya dengan pembentukan jelaga.Keselamatan Proses dan Perlindungan Alam Sekitar 85:430−40 doi: 10.1205/psep07020
CrossRef Google Scholar
[18] Shen G, Tao S, Wang W, Yang Y, Ding J, et al.2011. Pembebasan hidrokarbon aromatik polisiklik beroksigen daripada pembakaran bahan api pepejal dalaman.Sains & Teknologi Alam Sekitar 45:3459−65 doi: 10.1021/es104364t
CrossRef Google Scholar
[19] Agensi Antarabangsa untuk Penyelidikan Kanser (IARC), Pertubuhan Kesihatan Sedunia.2014. Ekzos enjin diesel dan petrol dan beberapa nitroarena.Agensi Antarabangsa untuk Penyelidikan Monograf Kanser mengenai Penilaian Risiko Karsinogenik kepada Manusia.Laporan.105:9
[20] de Oliveira Galvão MF, de Oliveira Alves N, Ferreira PA, Caumo S, de Castro Vasconcellos P, et al.2018. Zarah pembakaran biojisim di rantau Amazon Brazil: Kesan mutagenik nitro dan oxy-PAH dan penilaian risiko kesihatan.Pencemaran Alam Sekitar 233:960−70 doi: 10.1016/j.envpol.2017.09.068
CrossRef Google Scholar
[21] Wang X, Zhou L, Luo F, Zhang X, Sun H, et al.2018. 9,10-Endapan antrakuinon di ladang teh mungkin menjadi salah satu punca pencemaran dalam teh.Kimia Makanan 244:254−59 doi: 10.1016/j.foodchem.2017.09.123
CrossRef Google Scholar
[22] Anggraini T, Neswati, Nanda RF, Syukri D. 2020. Pengenalpastian pencemaran 9,10-antrakuinon semasa pemprosesan teh hitam dan hijau di Indonesia.Kimia Makanan 327:127092 doi: 10.1016/j.foodchem.2020.127092
CrossRef Google Scholar
[23] Zamora R, Hidalgo FJ.2021. Pembentukan naftokuinon dan antrakuinon oleh tindak balas karbonil-hidrokuinon/benzokuinon: Satu laluan berpotensi untuk asal 9,10-antrakuinon dalam teh.Kimia Makanan 354:129530 doi: 10.1016/j.foodchem.2021.129530
CrossRef Google Scholar
[24] Yang M, Luo F, Zhang X, Wang X, Sun H, et al.2022. Pengambilan, translokasi dan metabolisme antrasena dalam tumbuhan teh.Sains Persekitaran Keseluruhan 821:152905 doi: 10.1016/j.scitotenv.2021.152905
CrossRef Google Scholar
[25] Zastrow L, Schwind KH, Schwägele F, Speer K. 2019. Pengaruh merokok dan barbeku pada kandungan antrakuinon (ATQ) dan hidrokarbon aromatik polisiklik (PAH) dalam sosej jenis Frankfurter.Jurnal Kimia Pertanian dan Makanan 67:13998−4004 doi: 10.1021/acs.jafc.9b03316
CrossRef Google Scholar
[26] Fouillaud M, Caro Y, Venkatachalam M, Grondin I, Dufossé L. 2018. Anthraquinones.Dalam Sebatian Fenolik dalam Makanan : Pencirian dan Analisis, eds.Leo ML.Jilid.9. Boca Raton: CRC Press.ms 130−70 https://hal.univ-reunion.fr/hal-01657104
[27] Piñeiro-Iglesias M, López-Mahı́a P, Muniategui-Lorenzo S, Prada-Rodrı́guez D, Querol X, et al.2003. Kaedah baru untuk penentuan serentak PAH dan logam dalam sampel bahan zarah atmosfera.Persekitaran Atmosfera 37:4171−75 doi: 10.1016/S1352-2310(03)00523-5
CrossRef Google Scholar
Mengenai artikel ini
Petik artikel ini
Yu J, Zhou L, Wang X, Yang M, Sun H, et al.2022. 9,10-Pencemaran antrakuinon dalam pemprosesan teh menggunakan arang batu sebagai sumber haba .Penyelidikan Tumbuhan Minuman 2: 8 doi: 10.48130/BPR-2022-0008
Masa siaran: Mei-09-2022